Adv Sci(IF=14.1)上海同济大学&上海交通大学医学院等团队:HiST:通过多尺度融合深度学习利用组织学图像重建肿瘤空间转录组
了其作为临床常规工具的应用。近年来,人工智能(AI)方法尝试从H&E图像中直接预测空间基因表达谱(GEPs),以替代昂贵的ST检测。上开展,通过留一法交叉验证与多个公开模型对比,旨在证明HiST在基因表达预测精度(预期平均皮尔逊相关系数超0.70)、计算效率及临床任务表现(预后C-index达0.78,免疫响应预测准确率近0.80)上均显著优于现有方法,从而为。此外,现有方法普遍未充分验证预测结果
01
文献学习

今天分享的文献是由上海同济大学、上海交通大学医学院等团队于2026年3月在《Advanced Science》(中科院1区top。IF=14.1)上发表的研究”HiST: Histological Images Reconstruct Tumor Spatial Transcriptomics via MultiScale Fusion Deep Learning“即HiST:通过多尺度融合深度学习利用组织学图像重建肿瘤空间转录组,该研究提出一个名为 HiST 的多尺度融合深度学习框架,旨在利用常规HE染色组织学图像重建肿瘤的空间转录组(spatial transcriptomics, ST)。HiST通过提取组织图像中的形态学特征,预测肿瘤区域和空间基因表达谱(GEPs),并在多个癌种中实现了高精度预测。该模型在肿瘤区域识别、空间基因表达重建、患者预后分层、免疫治疗反应预测等方面均表现出优越性能,显著优于现有方法。
创新点:①提出多尺度融合卷积框架HiST,通过改进U-Net与ConvMixer模块,高效捕捉全局空间上下文与局部形态特征。②预测精度显著超越现有模型,平均Pearson相关系数达0.74,较第二名提升约两倍,实现高保真空间转录组重建。③首次实现从组织学图像预测免疫治疗疗效,并整合预后分析与肿瘤异质性评估,拓展了HE图像的分子信息挖掘能力。
临床价值:①规避空间转录组高昂成本,仅用常规HE染色图像即可推断高精度基因表达谱,降低临床应用门槛。②支持患者预后分层与免疫治疗反应预测,为个性化治疗决策提供可解释的分子依据。③从组织图像中识别肿瘤异质性与关键通路,辅助病理诊断与精准肿瘤学分析,提升诊疗一体化能力。
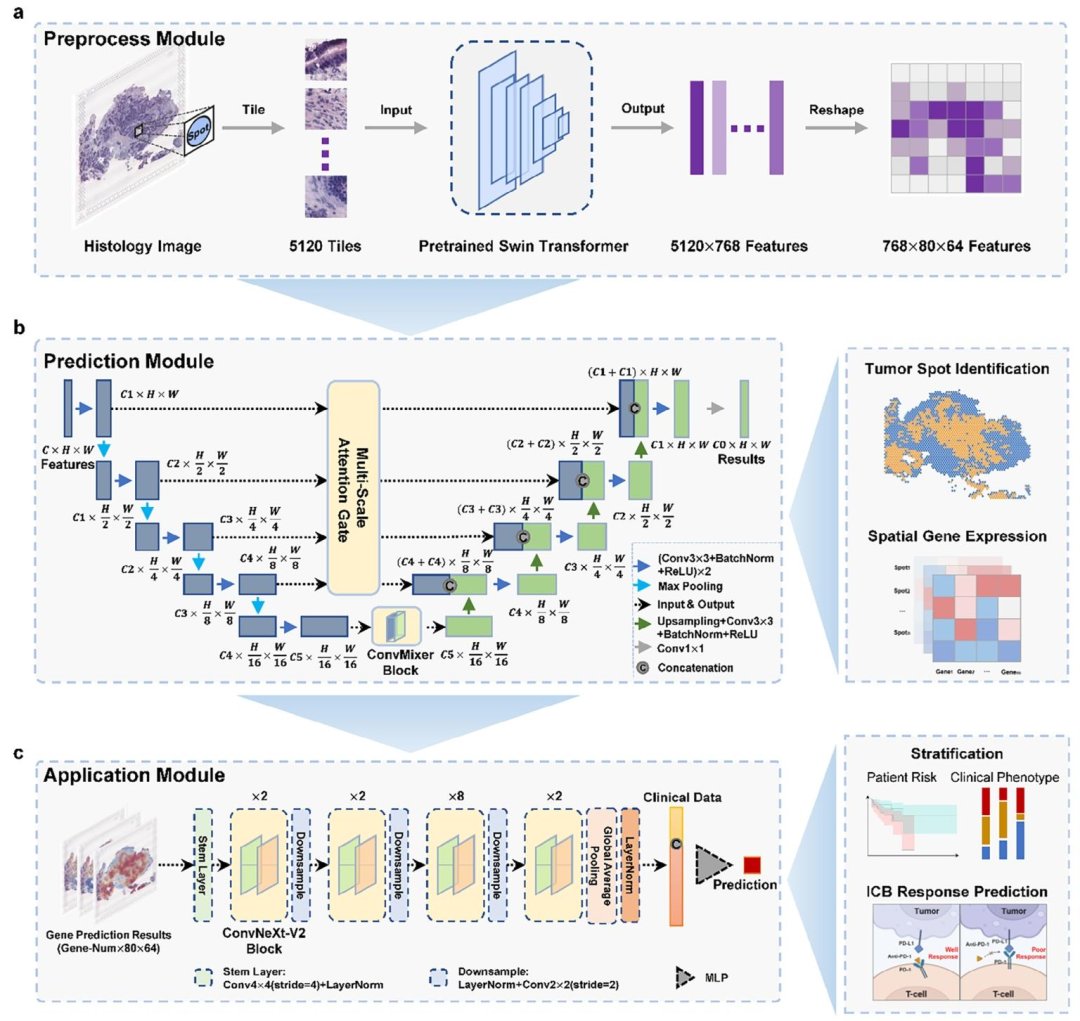
图 1:HiST框架示意图
a:预处理模块(Preprocess Module)
HE组织学全切片→按空间转录组斑点位置切分为5120个图像块→经预训练Swin Transformer(CTranspath)提取特征→重构为768×80×64空间特征图
b:预测模块(Prediction Module)
基于改进U-Net架构,编码器5层卷积+下采样,解码器对称上采样,加入多尺度注意力门跳跃连接与ConvMixer模块;双输出:
肿瘤区域识别(二分类掩码)
空间基因表达谱(逐基因空间表达矩阵)
c:应用模块(Application Module)
基于ConvNeXt-V2,输入HiST预测的空间转录组特征+临床数据;输出:
患者预后风险分层
免疫检查点阻断(ICB)治疗响应预测
02
研究背景和目的
研究背景
随着肿瘤精准医疗的发展,传统病理诊断仅依赖苏木精-伊红(H&E)染色图像,虽能揭示组织结构与细胞形态,却难以全面反映肿瘤微环境中复杂的分子调控异质性,且诊断结果易受病理医师经验与主观性影响。空间转录组学(ST)技术通过将基因表达与组织空间坐标相结合,为解析肿瘤异质性、免疫微环境及疾病机制提供了关键分子视角,但其高昂成本与长周期限制了其作为临床常规工具的应用。近年来,人工智能(AI)方法尝试从H&E图像中直接预测空间基因表达谱(GEPs),以替代昂贵的ST检测。然而,现有模型如ST‑Net、HisToGene、Hist2ST及IGI‑DL等存在明显局限:一方面,基于Vision Transformer(ViT)或图神经网络(GNN)的架构参数量大、易过拟合,尤其在小规模ST数据集上表现不佳;另一方面,它们对全局空间上下文与局部形态特征的融合不足,导致基因表达预测精度较低(平均皮尔逊相关系数仅约0.34)。此外,现有方法普遍未充分验证预测结果在下游临床任务(如预后分层、免疫治疗响应评估)中的可靠性,限制了其临床转化潜力。
研究目的
针对上述挑战,本研究旨在开发一个名为HiST(Histological Images reconstructs Tumor Spatial Transcriptomics)的新型深度学习框架,其核心目标是从H&E染色组织学图像中高精度重建肿瘤空间转录组谱,并系统验证其在肿瘤区域识别、异质性分析及临床预后预测中的实用性。HiST通过多尺度融合卷积架构,创新性地整合了三个模块:预处理模块利用Swin Transformer提取图像斑块特征并重构空间特征图,以保留全局空间关系与局部形态信息;预测模块基于改进的U‑Net与ConvMixer,实现肿瘤斑点分割和空间基因表达回归;应用模块采用ConvNeXt‑V2,将预测的GEPs用于患者生存分析和免疫治疗响应预测。研究在五种癌症类型(乳腺癌、结直肠癌、肝癌、肾癌、卵巢癌)的102张ST切片上开展,通过留一法交叉验证与多个公开模型对比,旨在证明HiST在基因表达预测精度(预期平均皮尔逊相关系数超0.70)、计算效率及临床任务表现(预后C-index达0.78,免疫响应预测准确率近0.80)上均显著优于现有方法,从而为将常规病理图像转化为可解释的分子图谱、推动空间信息辅助的精准肿瘤诊疗提供技术支撑。
03
数据和方法
研究数据
训练与验证数据:102张ST切片,涵盖5种癌种:
乳腺癌(BRCA,42例)
结直肠癌(CRC,25例)
肝细胞癌(HCC,13例)
肾透明细胞癌(KIRC,14例)
卵巢癌(OV,8例)
外部验证:TCGA数据库中的HE图像与RNA-seq数据;
免疫治疗数据:131例HCC患者(29例响应者,102例非响应者)的HE图像与临床数据。
技术方法
HiST框架结构:
预处理模块:提取HE图像中的补丁,使用Swin Transformer提取特征,构建空间特征图;
预测模块:基于改进的U-Net结构,引入多尺度注意力门控和ConvMixer模块,用于肿瘤区域分割和空间基因表达回归;
应用模块:基于ConvNeXt-V2结构,用于预后预测和免疫治疗反应预测。
模型训练策略:
小数据集:留一法交叉验证(LOOCV);
大数据集:5折交叉验证;
使用MSE损失(基因表达)和二元交叉熵损失(肿瘤区域)。
评估指标:
Pearson相关系数、Spearman相关系数;
AUC、IOU、Dice、F1、精度、召回率等;
C-index用于生存分析。
04
实验结果
肿瘤区域识别:
AUC最高达0.96(BRCA),各癌种平均准确率 > 0.80;
预测结果与病理学家注释高度一致。
空间基因表达预测:
平均Pearson相关系数为0.74,优于现有模型(如EGNv2仅为0.28);
在ACTB、FTL、UBC等关键基因上预测精度高达0.96以上;
在HER2和cSCC等非Visium平台上也表现优异。
肿瘤异质性分析:
HiST预测的GEPs可区分不同肿瘤亚克隆,与真实ST的CNV模式高度一致。
预后预测:
HiST预测的GEPs在TCGA五个癌种中均能显著分层高风险与低风险患者;
C-index最高达0.78(BRCA),优于Swin Transformer和ResNet50。
免疫治疗反应预测:
预测免疫治疗响应者的准确率为0.79,F1为0.81;
识别的差异基因与真实ST数据高度一致(重叠率44%-46%)。
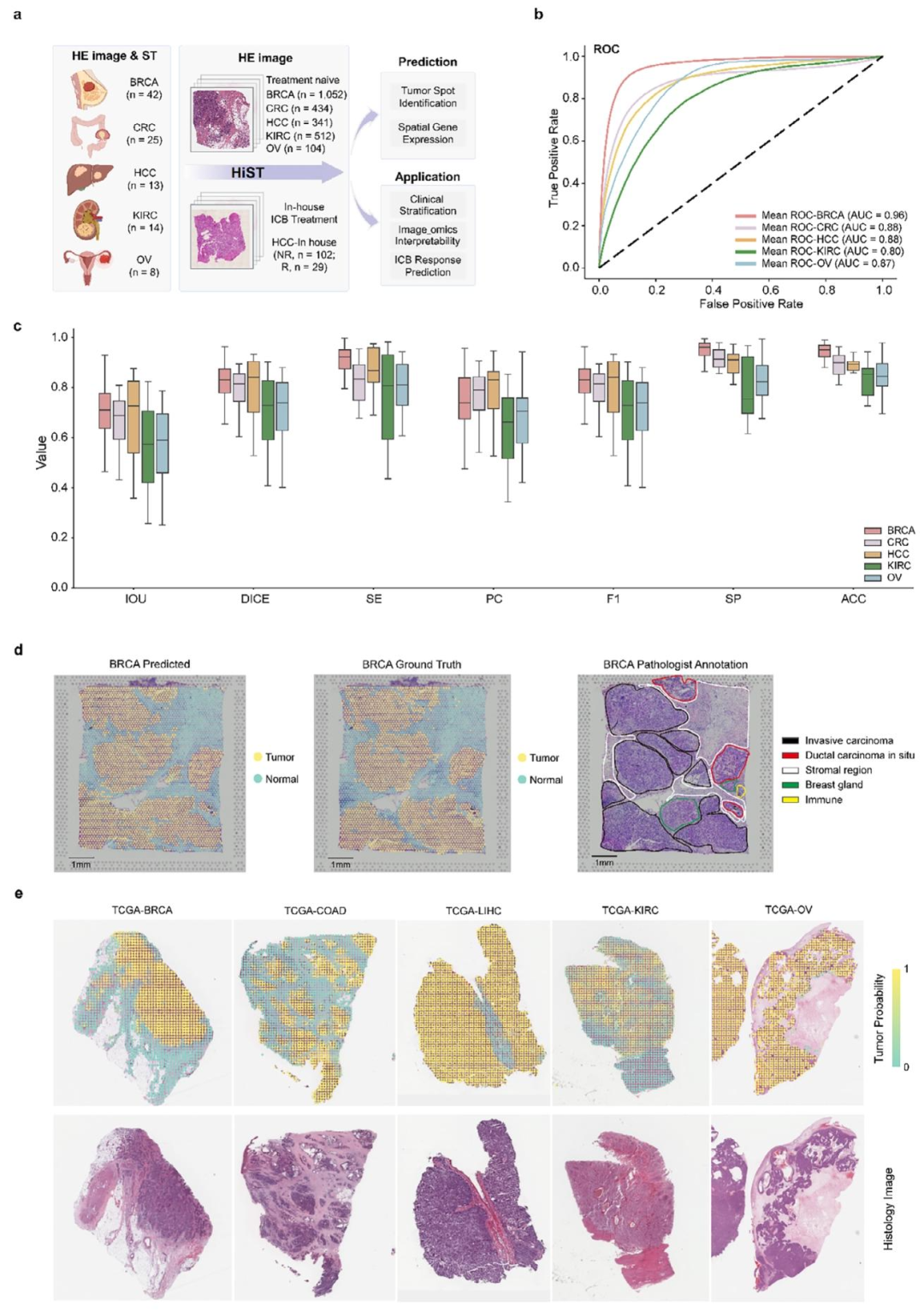
图 2:多癌种肿瘤区域预测结果
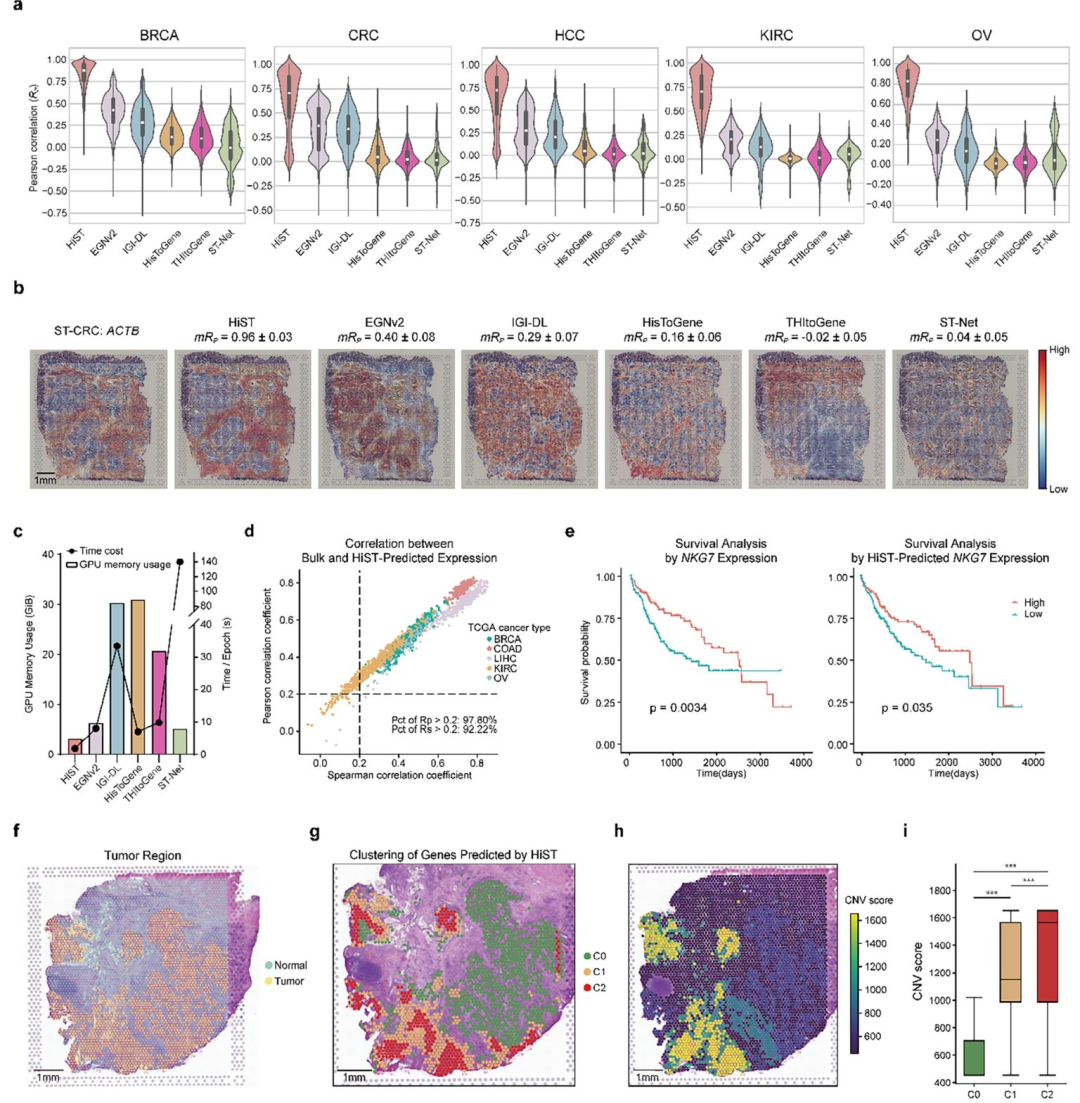
图 3:空间转录组基因表达谱重构性能
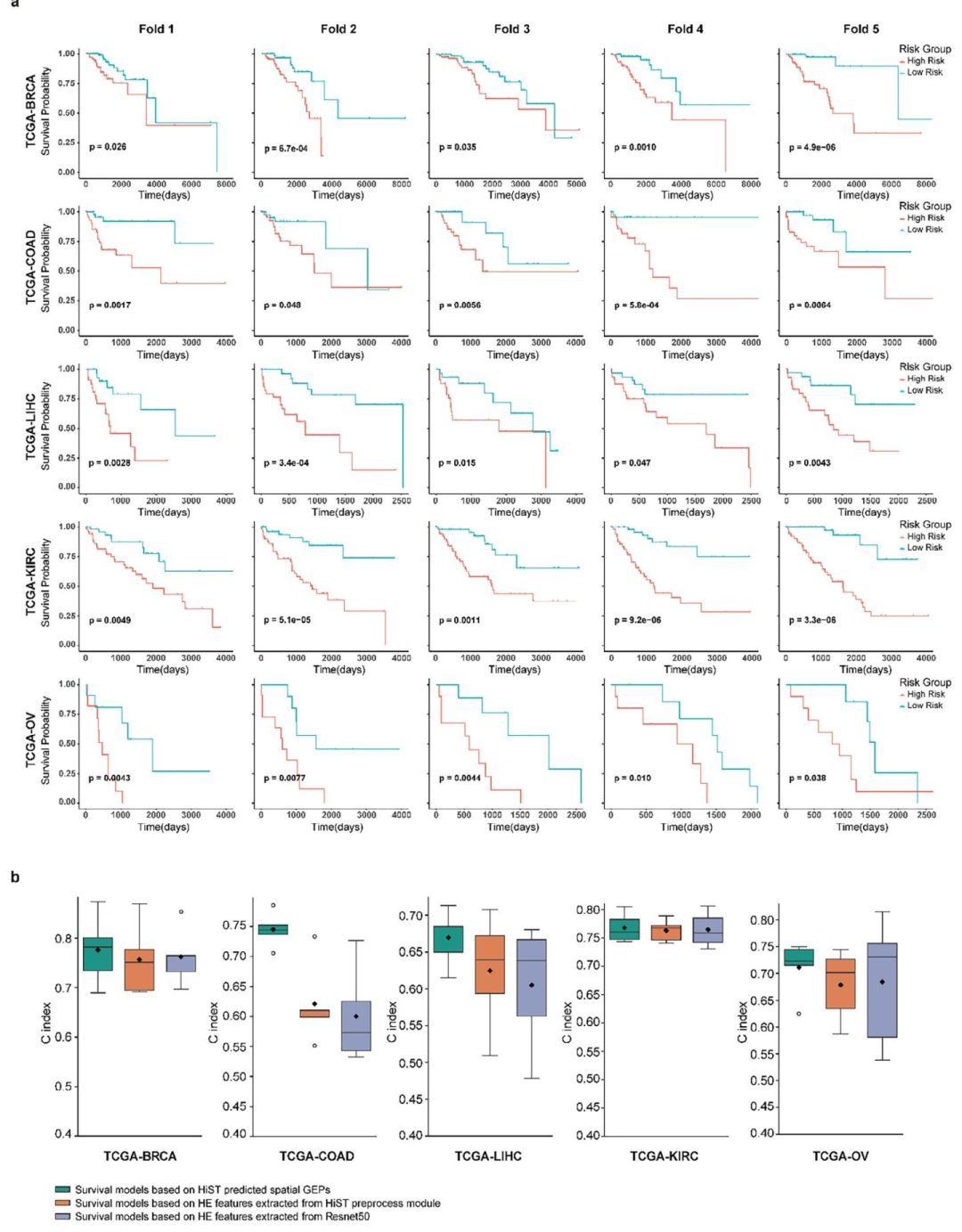
图 4:五癌种预后预测性能
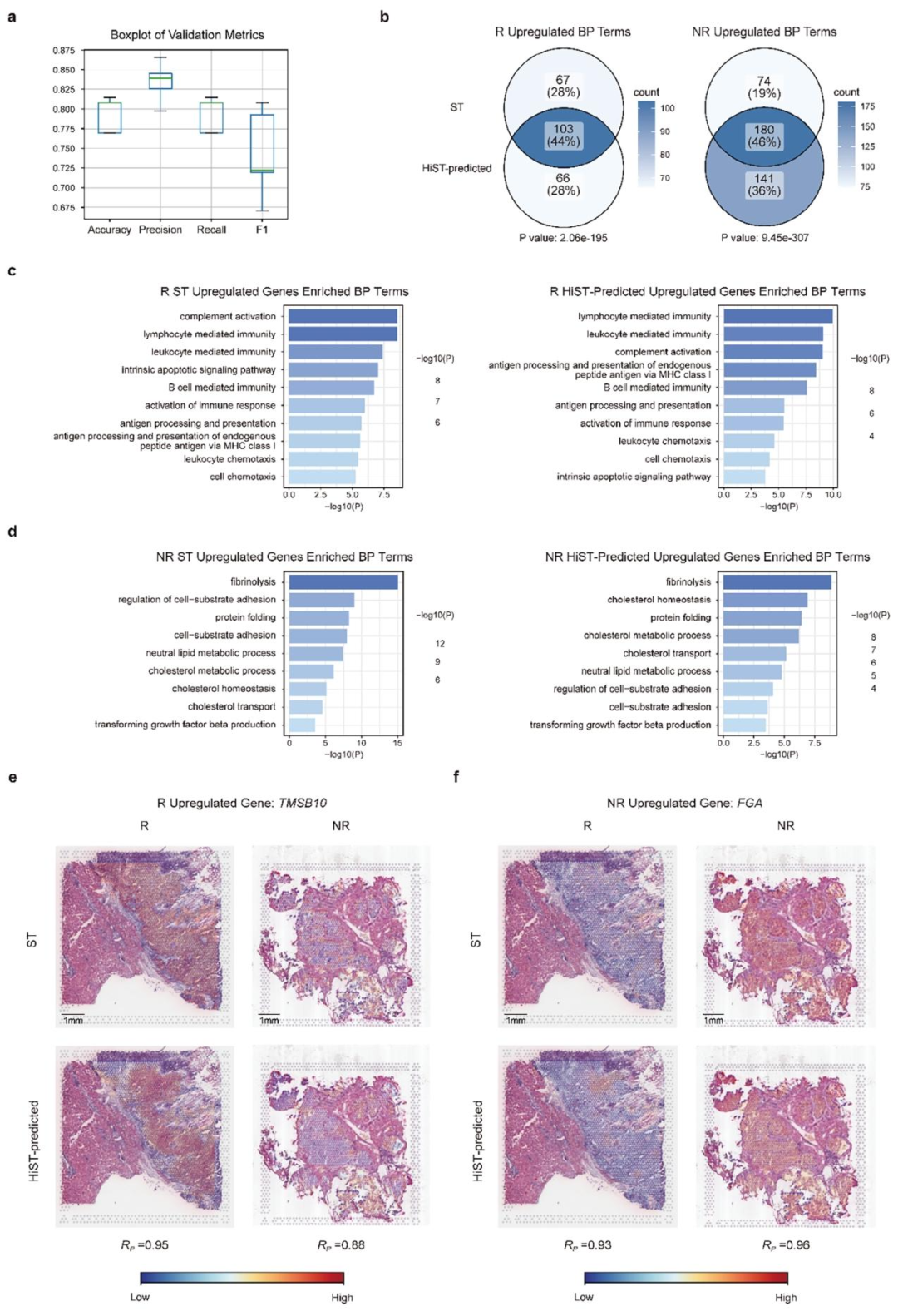
图 5:肝癌免疫治疗疗效预测
05
研究结论
该研究提出的HiST框架通过多尺度融合深度学习,成功从H&E染色组织学图像中高精度重建肿瘤空间转录组。其核心结论包括:①在肿瘤区域识别上,HiST在多种癌症类型中表现优异(如乳腺癌AUC达0.96),与病理学家注释高度一致;②在空间基因表达预测方面,HiST的平均皮尔逊相关系数达0.74,较现有模型提升约两倍,且计算效率更高;③预测的空间转录组谱能有效揭示肿瘤异质性(如区分不同CNV亚克隆),并在预后分层(如乳腺癌C-index达0.78)和免疫治疗响应预测(准确率0.79)中展现出显著临床应用价值;④HiST在多种独立数据集和平台上的泛化能力强,其预测表达与真实RNA-seq高度一致,为缺乏空间转录组数据的临床场景提供了低成本、可解释的分子替代方案。总体而言,HiST实现了从形态学到空间分子信息的跨尺度建模,为精准肿瘤学的临床转化提供了新工具。
参考文献:Li W, Zhang D, Peng E, Shen S, Alinejad-Rokny H, Liu Y, Zheng J, Jiang C, Ye Y. HiST: Histological Images Reconstruct Tumor Spatial Transcriptomics via MultiScale Fusion Deep Learning. Adv Sci (Weinh). 2026 Mar;13(13):e14351. doi: 10.1002/advs.202514351.
更多推荐
 已为社区贡献2条内容
已为社区贡献2条内容






所有评论(0)