基于深度学习的扩大的血管周围间隙(PVS)检测
实验结果表明,
深度学习在许多神经影像应用中已被证明是有效的。然而,在许多情况下,捕捉与小血管病病变相关信息的成像序列数量不足以支持数据驱动技术。此外,基于队列的研究可能并不总是拥有准确检测病变所需的最佳或必要的成像序列。因此,有必要确定哪些成像序列对精确检测至关重要。本研究介绍了一种用于检测扩大的血管周围间隙(ePVS)的深度学习框架,并旨在找到用于深度学习量化的最佳MRI序列组合。我们实现了一种有效的轻量级U-Net,适用于ePVS检测,并全面调查了SWI、FLAIR、T1加权(T1w)和T2加权(T2w)MRI序列信息的不同组合。实验结果表明,T2w MRI对于准确检测ePVS最为重要,而在深度神经网络中加入SWI、FLAIR和T1w MRI对准确性有微小改进,达到了最高的敏感性和精度(敏感性=0.82,精度=0.83)。与人工阅读相比,所提出的方法在最小时间成本下实现了相当的准确性。所提出的自动化管道能够从MRI扫描中实现稳健且高效的ePVS读取,展示了T2w MRI在ePVS检测中的重要性以及使用多模态图像的潜在好处。此外,该模型提供了全脑ePVS地图,相较于仅在几个脑区进行评分的方法,更有助于理解其临床关联。本文发表在Neuroimage: Reports杂志。(可添加微信号19962074063或18983979082获取原文及补充材料,另思影提供免费文献下载服务,如需要也可添加此微信号入群,思影提供脑影像数据分析及课程,如感兴趣也可添加微信咨询)。
关键词
MRI, 深度学习, 扩大的血管周围间隙
1. 引言
血管周围(或Virchow-Robin)间隙的扩大会是脑小血管病和血管周围排水通路功能障碍的表现(Doubal et al., 2010; Wardlaw et al., 2020)。血管周围间隙是充满液体的空间,围绕在脑内的动脉、小动脉、静脉和小静脉周围(Wardlaw et al., 2013)。这些空间通常是显微镜级别的,但随着年龄增长和/或病理的出现可能会变大并变得可见,即扩大的血管周围间隙(ePVS)(Hou et al., 2017; Potter et al., 2015b; Wardlaw et al., 2020; Wardlaw et al., 2013)。通常,ePVS在T2加权(T2w)磁共振成像(MRI)中,平行于成像平面时表现为亮或高信号的线性或曲线结构,垂直于成像平面时表现为椭圆形或点状(Wardlaw et al., 2013, 2020)。当血管周围间隙扩大时,它们在常规结构MRI中变得可见,直径通常小于3毫米,但在诸如基底神经节等区域可达到10-20毫米(Wardlaw et al., 2013)。尽管可以在T1加权(T1w)和T2w序列中评估ePVS,但使用T2w成像更容易可视化和量化(Ballerini et al., 2018; Potter et al., 2015a)。
许多检测/分割方法已经提出(Ballerini et al., 2018; Hou et al., 2017; Lian et al., 2018; Wang et al., 2016; Zhang et al., 2017),这些方法主要依赖T2w进行ePVS的检测/分割。然而,目前尚不清楚仅依赖单一模态如T2w的模型是否能处理类似脑病变如白质高信号(WMH)、腔隙性脑梗和梗死。WMH在T2w序列上表现为高信号,在T1w序列上表现为等信号或低信号;腔隙性脑梗是直径在3毫米到15毫米之间的圆形或卵圆形皮质下充液空腔,而梗死是在一个穿孔小动脉区域内近期梗死的神经影像证据(Wardlaw et al., 2013)。
在本文中,我们旨在评估一种基于深度学习的自动方法在使用多种MRI序列分割ePVS的可行性和有效性。我们使用MESA队列中一部分参与者的数据,这些数据由MESA房颤(AFib)附属研究在第六次检查时收集,提供了高质量的脑部MRI数据,具有临床场强和高空间分辨率(1毫米等方影像)。我们旨在评估在有或没有T2w MRI的情况下,以及T2w与其他MRI序列结合时的ePVS分割的准确性和可靠性。我们使用一种方法的变体,该方法之前使用MESA脑MRI数据开发,用于全自动检测基底神经节中的脑微出血和非出血性铁沉积(Rashid et al., 2021),并研究结合磁敏感加权成像(SWI)、流体衰减反转恢复(FLAIR)、T1w和T2w MRI序列信息的最佳策略。人类专家的ePVS分割结果作为模型训练的黄金标准。
自动化在大型队列研究中是理想的,因为它提高了可行性、重复性并减少了人为错误(Hurtz et al., 2019)。准确且可靠的方法对于从大型队列中提取丰富的数据集以研究与人口统计、认知和血管风险因素的关联(Habes et al., 2016a; Habes et al., 2016b; Habes et al., 2021),或改进新方法的开发至关重要(Liu et al., 2020; Liu et al., 2021)。
据我们所知,本研究是首批全面评估使用多模态成像进行ePVS检测的深度学习研究之一。本文的主要贡献包括:
1.开发了一种结合数据融合的有效深度学习方案,用于准确的ePVS分割。
2.将所提出的模型应用于全脑,而不是选择性的区域。
3.研究了使用不同序列以达到最佳性能的效果。
2. 相关工作
以前的ePVS分割方法通常采用传统的机器学习技术,例如血管增强滤波器(Ballerini et al., 2018)和支持向量机(SVM)(González-Castro et al., 2017)。Ballerini等人在T2对比MR图像上训练了一个模型(Ballerini et al., 2018),并通过分类评分进行评估(Potter et al., 2015a)。González-Castro等人将基于视觉词汇包描述符的SVM分类器应用于T2加权MR图像,重点是基底神经节(González-Castro et al., 2017)。Wang等人开发了一种半自动计算方法,在强度归一化的T2w MRI上提取双侧卵形基底神经节上的ePVS(Wang et al., 2016)。同时,一些研究利用手工特征作为预测指标,例如Boespflug等人使用信号强度和形态特征,包括宽度、体积和线性(Boespflug et al., 2018),而Ramirez等人使用一组局部强度阈值来量化血管周围间隙(Ramirez et al., 2015),Zhang等人提出了一种基于血管特征的结构化学习方法,用于使用T2w数据进行3维ePVS分割(Zhang et al., 2017)。此外,为了促进这些模型,Sepehrband等人结合了T1和T2w图像以增强PVS对比度,提高可见性(Sepehrband et al., 2019)。
随着深度学习技术的成功(Liu et al., 2021;Mou et al., 2021;Song和Liu, 2021;Yin et al., 2019),一些深度神经网络模型被提出用于ePVS分割。例如,Boutinaud等人开发了一种基于自动编码器和U形网络的深度学习算法,用于使用T1加权MRI数据进行深白质和基底神经节的3维ePVS分割(Boutinaud et al., 2021),Lian等人提出了一种使用7T T2加权MRI进行高效ePVS分割的全卷积神经网络(Lian et al., 2018),Dubost等人实现了用于中脑、海马体、基底神经节和半卵圆中心的独立卷积神经网络,训练于T2对比MRI以量化PVS(Dubost et al., 2019),Sudre等人重新设计了基于区域的卷积神经网络模型,以共同检测和表征与年龄相关的神经血管变化标志(Sudre et al., 2019),Jung等人提出了一种深度3维卷积神经网络,具有跳跃连接的密集连接网络,用于7T MRI的ePVS增强(Jung et al., 2019)。总体而言,这些工作没有研究如何充分利用不同信息源来基于深度数据驱动技术改进全脑的ePVS检测。此外,这些先前的研究大多使用7T MRI,而7T MRI在临床中的可用性较低,3T MRI更为常规且广泛可用,因此,针对3T MRI设计的深度学习模型是更具成本效益的选择。
3. 材料和方法
所提出方案的关键点是深度融合不同MRI序列的信息。整个过程的概述总结在图1中。首先,将标准图像处理技术应用于MESA队列子集的不同序列的原始MRI数据,包括不均匀校正、重新定向、平滑和过滤、脑部掩膜和去颅骨处理,然后进行灰质(GM)、白质(WM)和脑脊液(CSF)分割。然后,将参与者的MRI配准到SWI。预处理后的MRI数据进行手动分割,以获得用于模型训练的真实数据,并使用留一法交叉验证。
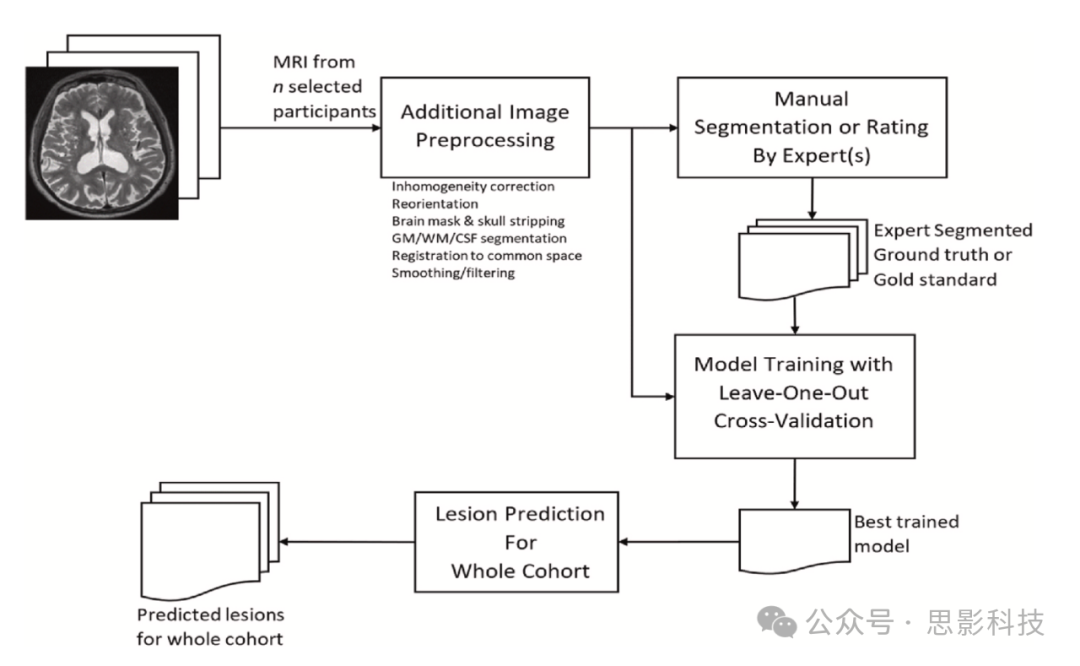
图1. 提议的ePVS检测/分割程序概述
3.1 数据
训练数据包括21名参与者,随机选自MESA队列。对于T1w、T2w和FLAIR图像,MESA研究在6个不同站点使用西门子扫描仪(Skyra配20通道头线圈,Prisma和Prisma Fit配32通道头线圈)收集了3D等方MRI扫描。我们的训练数据包括来自所有这些站点和所有扫描仪型号的参与者,从而确保了在MESA队列内的普遍适用性。MRI扫描参数如表1所示。
表1. MRI扫描仪参数
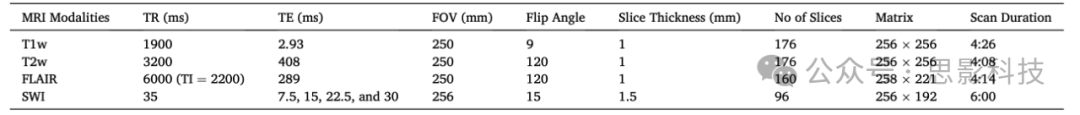
21名参与者的年龄范围为64至94岁,平均年龄为78.7岁,其中12人为女性。每位参与者的平均总病灶数超过683个。这些参与者的ePVS分割由一位经验丰富的放射科医生(JBW)进行,作为模型训练的真实数据(见补充材料表S1)。手动分割使用共配准的T2w、T1w和FLAIR图像进行,以确保地面真实数据中减少出现假阳性(例如WMH或腔隙性脑梗)的可能性(Wardlaw et al., 2013)。完成整个大脑ePVS手动分割的平均时间约为每位参与者24小时。对于模型训练和评估,我们使用FLAIR、SWI、T1w和T2w图像,这些图像经过重新定向、N4偏场校正(Avants et al., 2009)和去颅骨处理(Doshi et al., 2016)。SWI相位掩模是使用尺寸为64 × 64的高通滤波器从相位图像生成的,以去除伪影,SWI通过将幅度图像与相位掩模相乘生成(Haacke et al., 2009; Haacke et al., 2004)。为了生成参考注释和机器推理,只使用回波时间最短的SWI图像(TE = 7.5 ms),因为使用较长回波时间采集的SWI图像噪声更大。不同序列上的ePVS示例如图2所示。本研究使用的MRI扫描具有高空间分辨率,使得检测小的ePVS成为可能,尽管在临床环境中,切片厚度较大以减少扫描时间,因此在切片之间发生的小病灶可能不可见。
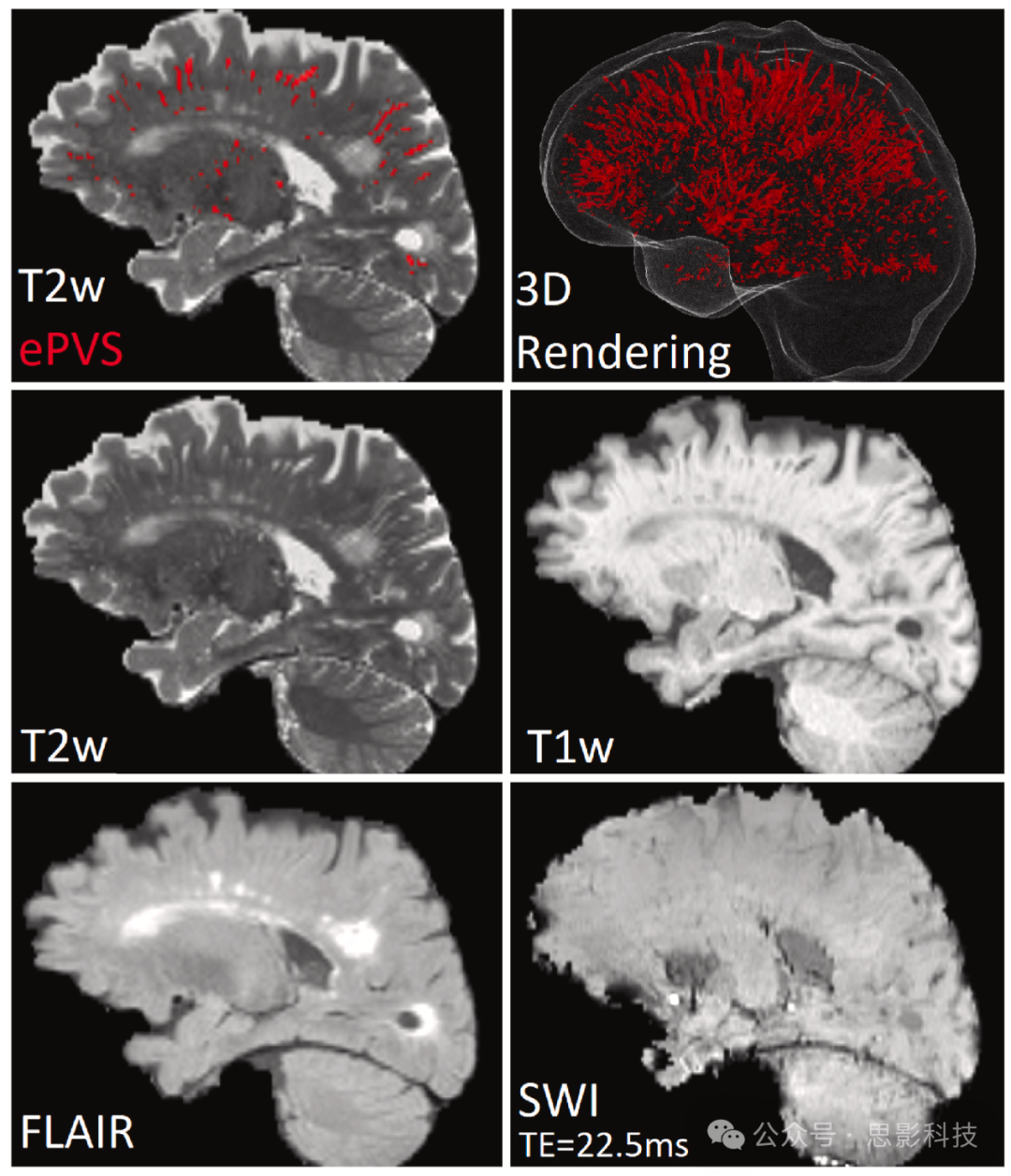
图2. 不同MRI序列中ePVS的示例
从上到下,从左到右:
a) 标记有ePVS区域的T2w图像,标记为红色。
b) ePVS的3D渲染,标记为红色。
c) 未标记标签的原始T2w图像。
d) 对应的T1w图像。
e) 对应的FLAIR图像。
f) 回波时间为22.5 ms时对应的SWI图像。
假设
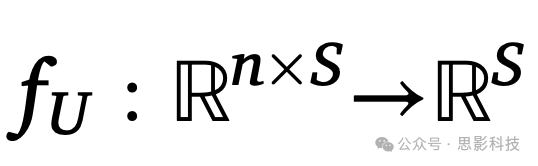
是一个具有一组可学习参数U的非线性函数,其中n是使用的MRI序列数量,S是图像的大小,f将n张图像映射到体素级标签,指示体素是否包含ePVS。在本研究中,fU被实现为一个多通道深度神经网络(Rashid et al., 2021),这是标准U-Net(Ronneberger et al., 2015)的变体,并已被证明在处理小病灶方面优于传统U-Net(Rashid et al., 2021)。典型的U-Net由下采样或编码路径和对称的上采样或解码路径组成。下采样路径由一系列卷积块、归一化块、激活块和池化块组成。上采样路径由一系列卷积块、归一化块、激活块和转置卷积块组成。每个对应的下采样路径和上采样路径的特征图被连接起来。
所提出的方案可以对来自不同序列的信息进行深度融合。ePVS检测/分割模型通过多通道U-Net融合来自T2w、SWI、FLAIR和T1w图像的信息。它被设计为可扩展的方式,即仅使用T2的网络基本上是单通道U-Net,可以很容易地扩展以包含多种序列。人工专家的手动分割结果被用来通过留一法交叉验证训练深度学习模型。具体来说,在留一法交叉验证的每次迭代中,我们使用20名受试者的数据进行网络训练,使用1名受试者的数据进行测试。此外,在用于训练的20名受试者中,有4名专门用于训练内验证。
每个三维(3D)扫描被切割成二维(2D)轴向切片,这些切片通过几何变换组合(如旋转、平移、上下和左右翻转)进行数据增强。在每次实验中,轴向T2w切片(以及其他MRI中的对应轴向切片)和对应的轴向真实切片都会进行增强。对于平移,生成了一组范围在[-45, 45]之间的两个随机浮点数tx和ty(表示每个轴的平移量),用于平移图像切片和对应的真实切片。这个范围是通过经验选择的,以确保大部分大脑在平移后的图像中仍然可见。每个轴共生成10个随机浮点数,导致每个切片有10 × 10 = 100次平移。对于旋转,生成了一组范围在[1, 60]之间的随机浮点数d(表示旋转角度),并使用+d和-d对图像切片和真实切片进行旋转。裁剪区域位于图像矩阵外的部分使用边缘值填充。共使用16个随机浮点数,导致16 × 2 = 32次旋转。相同的变换集也应用于翻转的图像。例如,一个具有96个轴向切片的T2w MRI图像在数据增强后产生23,880个轴向切片。这些增强数据作为数据样本输入到神经网络中。
我们旨在训练多类模型,其中预测类别为背景和ePVS,使用以下成像序列组合:(1) 仅T2w,(2) T2w和FLAIR,(3) T2w、T1w和FLAIR,(4) T2w、T1w、FLAIR和SWI,(5) T2w和T1w,(6) 仅FLAIR,(7) 仅T1w,(8) T1w和FLAIR。深度学习模型的训练时间为3-8天。一旦模型训练完成,训练后的模型可以在不到30秒内预测全脑的ePVS。
这些模型的准确性基于三个参数:敏感性 (S)、精度 (P) 和幅度准确性 (A),其定义如下:

其中,TP 是真阳性数,FN 是假阴性数,FP 表示假阳性数。我们还选择了一些对小病灶(如 ePVS)有效的指标,这些病灶的形状信息和体积非常重要。ePVS 可以小到一个体素。分析包括 Bland-Altman 图和 ePVS 数量和体积(预测与专家标注数据)的散点图,以及基于病灶质心的敏感性和精度。我们还使用组内相关系数(ICC)(Shrout 和 Fleiss, 1979)、体积相似性(Ramaswamy Reddy、Prasad 和 Reddy, 2013)、接收者操作特征曲线下的面积(AUC)、Hausdorff 距离(Rockafellar 和 Wets, 2009)和 Mahalanobis 距离(Xiang 等, 2008)来评估性能。对于 ICC,我们使用了 Shrout 和 Fleiss (1979) 的方法,采用双向随机模型、绝对一致性、单次测量。Hausdorff 距离计算对应于真实标签和分割结果的两组点之间的距离,而 Mahalanobis 距离是一种多变量距离度量,用于衡量一个点和一个分布之间的距离,特别适用于高度不平衡的数据集上的分类。平均指标是通过对所有受试者进行平均获得的,例如,假设 Si 是通过测试受试者 i (i=1,2,...,21) 获得的敏感性,那么平均敏感性为:
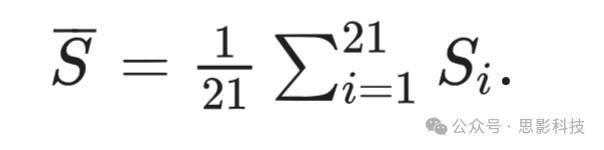
4. 结果
所有受试者的平均评估指标及其标准误,包括敏感性、精度、幅度准确性、ICC、体积相似性、AUC、Hausdorff 距离和 Mahalanobis 距离,如表2所示。结果表明,T2w MRI 是信息量最大的单一序列,在多个指标上表现最佳,并且在某些测量中接近最优。对于大多数测量,T2w、FLAIR、T1w 和 SWI 的组合达到了最佳性能。将 SWI 添加到其他 3 个序列的组合中总体增益较小,但改善了 ICC。
表2. 不同序列组合的受试者评估。最佳分数标记为红色,第二好分数标记为蓝色。对应的标准误在适用时显示。
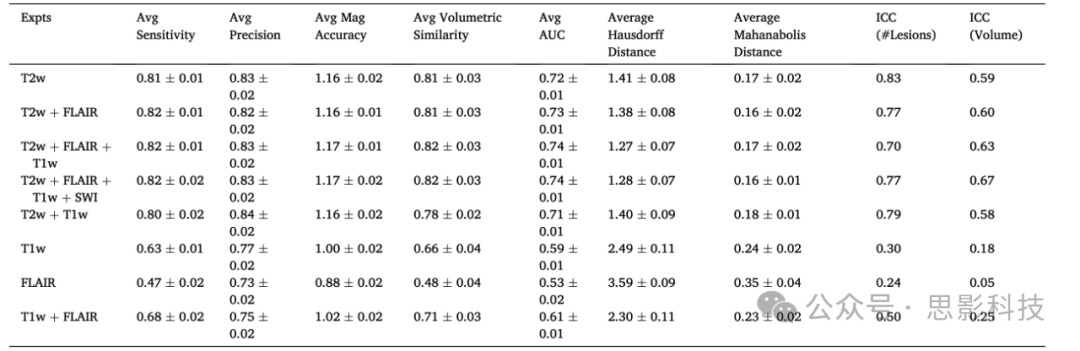
图3展示了预测病灶数量与真实病灶数量之间的相关性。使用T2w可以达到最高的相关性。图4绘制了所有参与者的(S, P)点对,表明通过包含T2w、FLAIR和T1w,模型可以达到最高的幅度准确性,这在图中
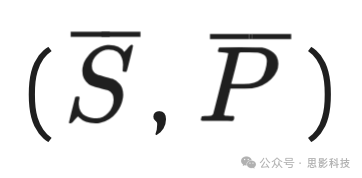
与(0, 0)之间的距离反映出来,其中
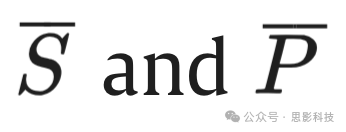
分别是中位敏感性和中位精度。图5显示了病灶数量的Bland-Altman图,表明使用仅T2w时,预测与金标准之间的平均差异以及平均值周围的随机波动达到最小,并且在结合其他序列时保持较低水平。图6展示了预测病灶体积与真实体积之间的相关性,重申了使用T2w进行ePVS分割的重要性。图7显示了病灶体积的Bland-Altman图,表明T2w、FLAIR、T1w和SWI的组合比仅使用FLAIR和T1w可以获得更好的结果,因为当结合T2w、T1w、FLAIR和SWI时,平均差异和波动最小,并且当包含T2w时,这些差异显著减小。
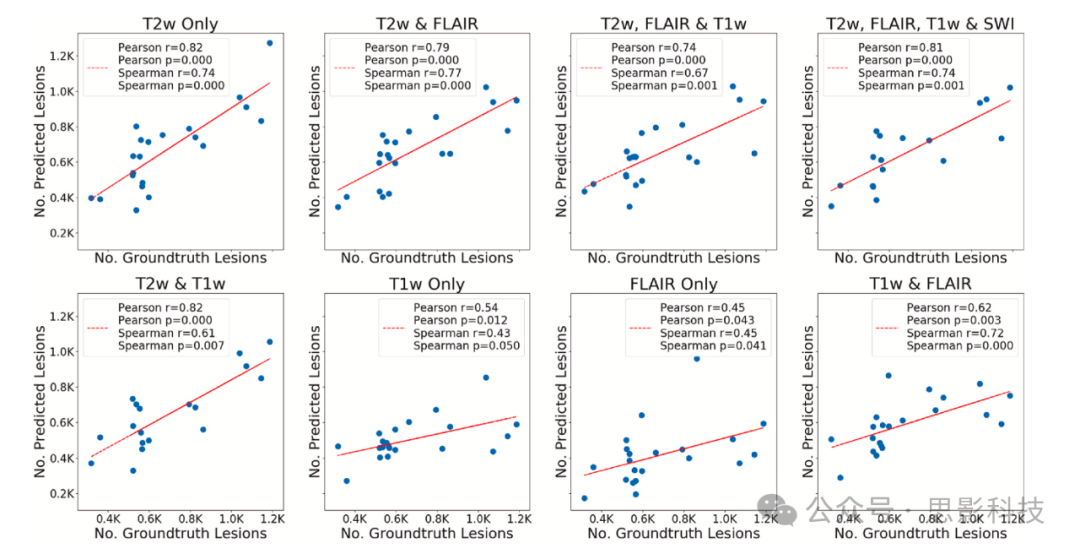
图3每位受试者的真实ePVS数量与预测ePVS数量的散点图,基于此计算Pearson相关系数和Spearman相关系数(r)及相应的p值(p)。
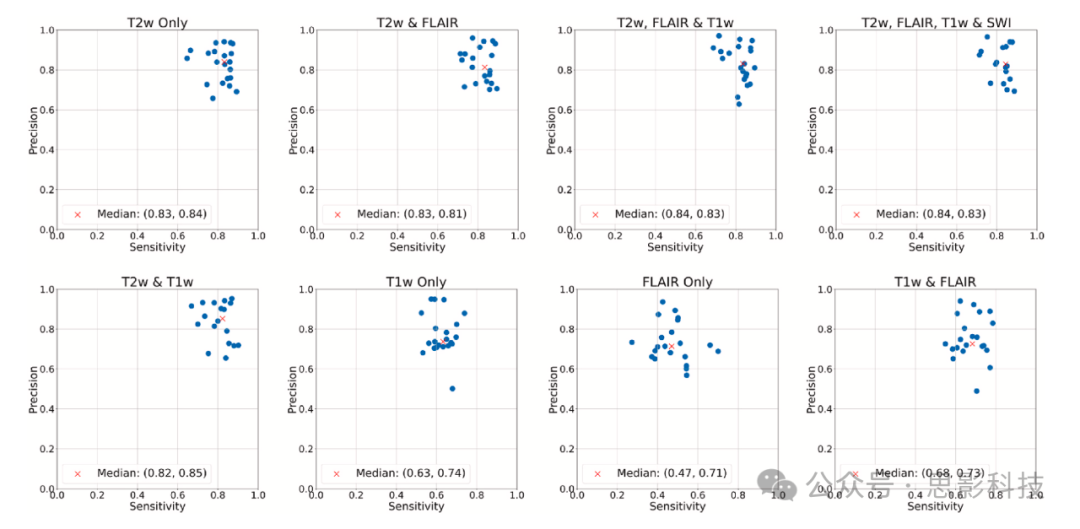
图4每位受试者的敏感性与精度的散点图以及不同序列组合的相应(中位敏感性,中位精度)。
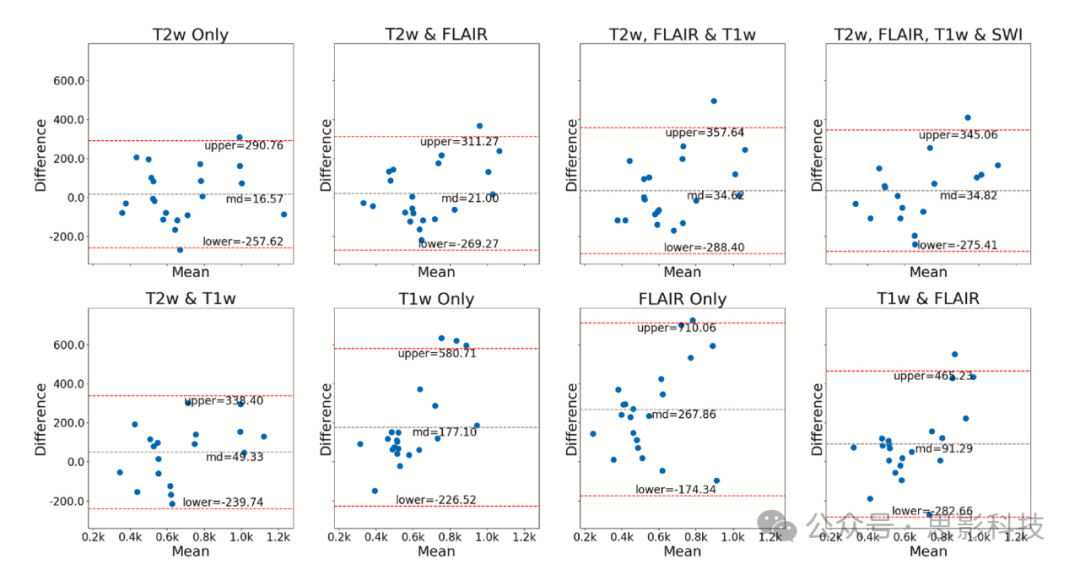
图5不同序列组合下的ePVS数量的Bland-Altman图。图显示了预测ePVS数量与真实ePVS数量之间的差异。
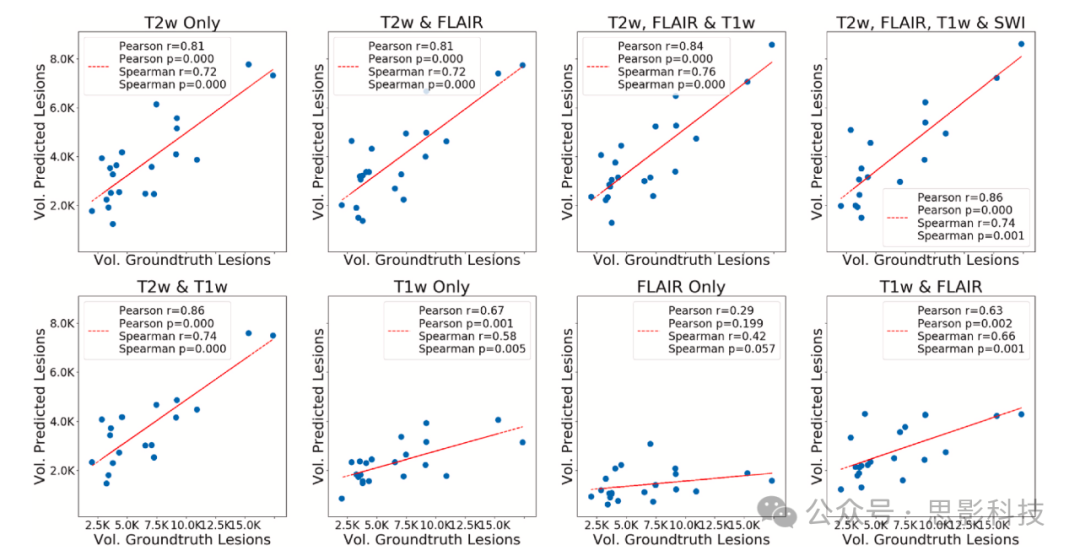
图6每位受试者的真实ePVS体积与预测ePVS体积的散点图,基于此计算Pearson相关系数和Spearman相关系数(r)及相应的p值(p)。
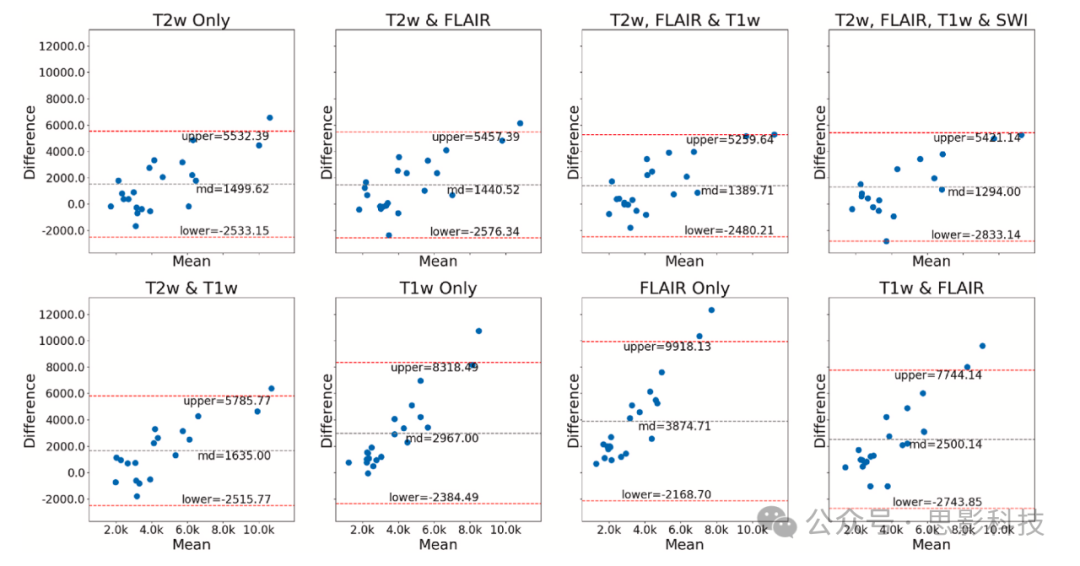
图7不同序列组合下的ePVS体积的Bland-Altman图。图显示了预测ePVS体积与真实ePVS体积之间的差异。
基于这些观察,我们可以看到,尽管T1和FLAIR是更标准的研究序列,但仅使用这两种序列对ePVS的评级远不如包含T2w准确,且结合其他序列并没有显著改善结果。然而,利用来自不同模态的信息使模型能够有效区分ePVS和类似物(如白质病灶和腔隙性脑梗),如图8所示。
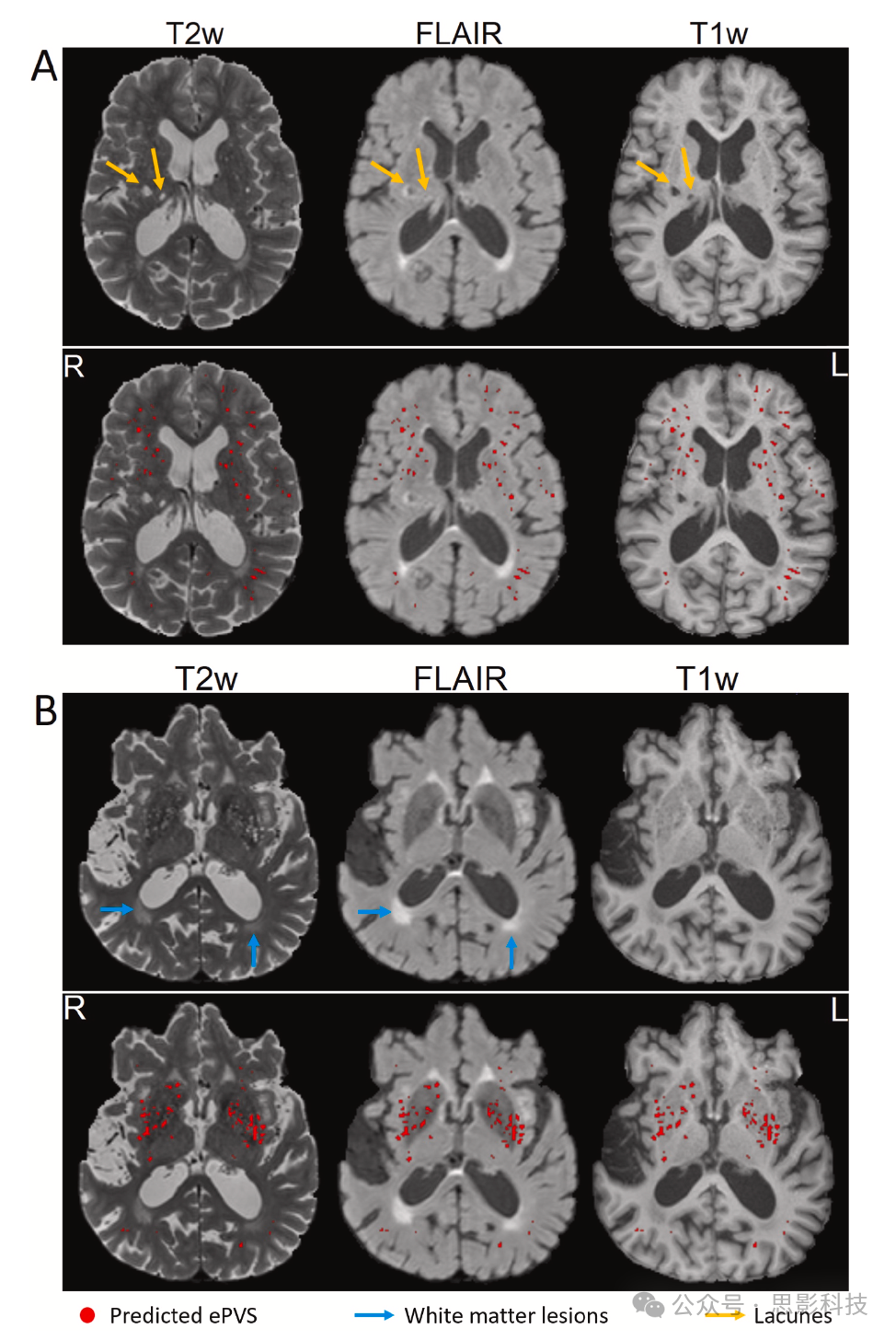
图8在T2w、FLAIR和T1w图像上同时存在白质病灶和腔隙性脑梗的情况下预测的ePVS示例。所提出的模型能够区分ePVS与这些类似物。
5. 讨论与结论
扩大的血管周围间隙(ePVS)作为脑健康和疾病(包括脑血管疾病)的亚临床生物标志物日益受到关注,因此其量化对研究界具有重要意义。手动量化单个ePVS极其耗时(Ramirez et al., 2015;Wang et al., 2016),且依赖于操作人员,并可能无法准确反映ePVS的真实负担。数据驱动的自动系统,包括深度学习模型,为从脑MRI扫描中生成稳健、可重复和快速的ePVS量化提供了一个有前途的方法,当训练数据集有限时,轻量级网络也足以实现准确预测(Peng et al., 2021)。
由于存在类似物如腔隙性脑梗和白质病变,自动ePVS量化具有挑战性,这些类似物可能导致假阳性测量。此外,在许多情况下,神经影像数据样本数量不足以支持数据驱动系统。这些问题在最近发表的深度学习方法中仍然存在。总体来说,有几个限制:1)单一模态是否足够信息丰富以进行ePVS量化仍然是个问题;2)尚未探讨结合不同序列的优势;3)现有方法通常使用7T MRI,而3T MRI在实践中更为可用和可接近;4)现有方法仅应用于选择性区域而非整个大脑。
为解决这些问题,本研究旨在通过联合利用不同序列,充分利用可用的3T MRI数据,并在深度学习框架中研究融合不同序列信息的最佳策略,用于全脑ePVS分割。特别是,由于数据样本数量通常有限,充分利用现有数据尤为重要,不同序列信息的融合可能是一种有效的解决方案。深度学习模型采用轻量级多通道U-Net变体,专为该应用量身定制。实验结果表明,T2w、FLAIR、T1w和SWI的组合可获得最佳分割性能,而单独使用T1w的性能比单独使用T2w的差。我们的结果表明,如果对ePVS的量化感兴趣,前瞻性研究应在脑MRI协议中包含T2w成像。由于T1w图像在脑组织分割中的实用性,在研究中更为普遍,但应预期其在ePVS量化中的准确性较低。
对于区域评估,我们基于现有的多图集区域分割利用集成(MUSE)(Doshi et al., 2016)得出几个区域,如补充材料的图S3所示。基于这些区域,我们在所有实验中对每个个体区域进行了相同的敏感性和精度计算。包括平均敏感性和精度等指标见补充材料表S2至S8。可以看到,在基底神经节中,所有实验的敏感性和精度都很高,即使仅使用T1或FLAIR。这表明我们可以仅使用T1和/或FLAIR在基底神经节中获得可靠且准确的ePVS读数。另一方面,我们看到海马和颞区的敏感性和精度较差。这是因为这些区域中存在的血管导致了假阳性。目前,最具临床相关性的ePVS读数区域是基底神经节、半卵圆中心和可能的中脑(Wardlaw et al., 2013,2020)。因此,我们的实验表明,即使在没有T2w的情况下,我们的模型也能在基底神经节和半卵圆中心做出准确的预测。
在这项工作中,我们选择了2D切片而不是3D,因为真实的ePVS标签是为每个切片单独手动标注的。尽管理论上使用3D样本可以利用相邻切片的上下文,但实际上当真实标签是逐切片手动生成时,相邻切片之间的这种连接可能很弱甚至具有误导性。从这个角度来看,使用2D数据集的主要好处是它可以更好地符合真实世界专家分割标签的特征。这可能是为什么在一些之前的工作中,2D数据集被证明优于3D数据集的原因(Srikrishna et al., 2022)。另一个实际原因是使用2D切片而不是3D图像是3D深度学习模型需要指数级更大的GPU内存来容纳所有参数。较小的模型可能适合商用GPU内存,但可能无法提取有效学习和分割所需的特征。
尽管我们使用的数据集是MESA脑MRI研究中第六次检查的一部分,并具有可用的真实数据,但我们通过在评估模型时执行留一法交叉验证尽可能减轻了过拟合的问题。我们的交叉验证策略显示出对可用数据集的良好泛化性,但使用外部数据集的额外实验可能会提高我们模型的泛化性。然而,这带来了挑战,即其他研究通常招募有病理的参与者,可能不包括类似的MRI序列如T2w、FLAIR和SWI,并且可能没有专家分割的ePVS标签。
总之,我们所提出的自动化管道能够从MRI扫描中实现稳健且高效的ePVS读取,展示了T2w MRI在ePVS检测中的重要性以及使用多模态图像的无显著益处。这也可能提供一种潜在的方法来缓解数据样本限制带来的问题。自动化管道将有助于在MESA中生成丰富的变量集,从而使得能够研究ePVS与其他风险因素的关系。本研究的一个局限是只有一位专家的手动ePVS分割数据可用。
补充材料:
Susceptibility-Weighted Imaging
SWI图像是通过Haacke等人(Haacke, Mittal, Wu, Neelavalli, & Cheng, 2009; Haacke, Xu, Cheng, & Reichenbach, 2004)的方法生成的。对原始相位图像应用空间窗口大小为64x64的同调高通滤波器生成负相位掩模。然后将此掩模提升到4次幂并与幅度图像相乘。在这项工作中,我们使用了回波时间最短(TE=7.5ms)的SWI图像。使用较长TE的一个副作用是图像质量下降。诸如鼻窦腔和颅底等区域的空气-组织界面的存在可能导致生成的SWI中出现失真/伪影(残余相位包裹误差)。此外,ePVS在较短TE的SWI图像上具有更好的对比度。补充图S1展示了在不同TE下采集的SWI图像中的ePVS示例。
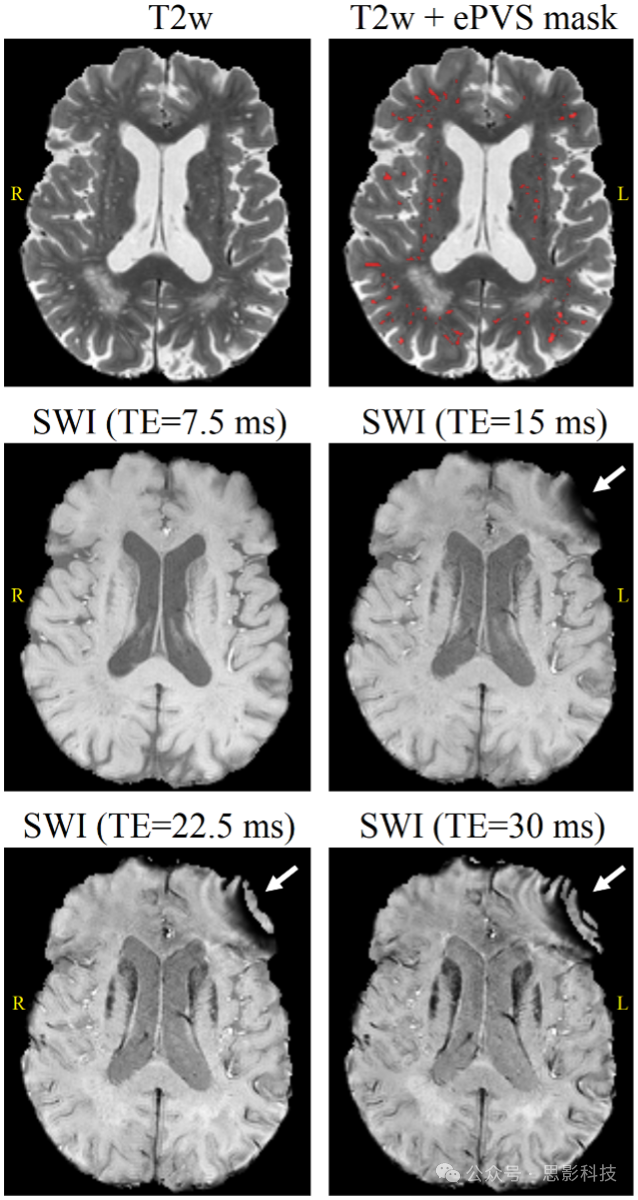
图S1 在不同回波时间(TE)下T2w和磁敏感加权成像(SWI)上看到的扩大的血管周围间隙(ePVS)。使用较长TE采集的SWI易受到伪影的影响,例如残余相位包裹误差(白色箭头)。
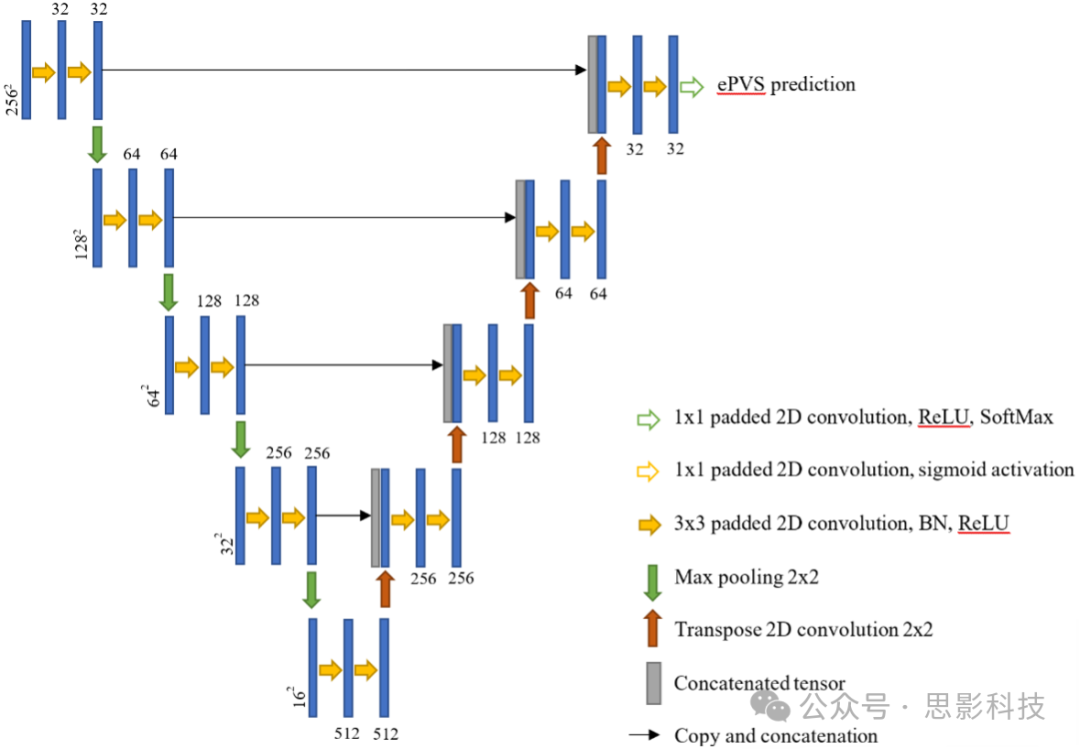
图S2 用于多模态MRI分割扩大的血管周围间隙的深度学习架构。
MESA队列
多种族动脉硬化研究(MESA)是一项研究亚临床心血管疾病特征(通过无创检测发现的疾病在产生临床症状和体征之前)和预测其进展为临床明显心血管疾病的风险因素的研究,涉及6,814名年龄在45-84岁之间的男女。整个参与人群中,38.5%为白人,27.7%为非裔美国人,22%为西班牙裔,11.8%为亚洲人,主要是华裔。该队列从六个现场中心招募,并对冠状动脉钙化、心室质量和功能、流量介导的内皮舒张功能、颈动脉内膜-中层厚度和颈动脉内回声透亮区的存在、下肢血管不全、动脉波形、心电图测量、标准冠状动脉风险因素、社会人口因素、生活方式因素和心理社会因素进行了表征。除了六个现场中心,该研究还涉及一个协调中心、一个中央实验室和用于计算机断层扫描(CT)、磁共振成像(MRI)、超声波、视网膜摄影和心电图的读取中心。协议开发在前18个月进行,工作人员培训和试点测试在每次检查前进行。第一次检查持续了25个月,随后进行了四次随访检查:分别为17个月、18个月、21个月和22个月的检查期。整个研究过程中,每9-12个月会联系参与者一次,以评估临床发病率和死亡率。该研究最初资助了9.5年,现场中心、协调中心、MRI读取中心和中央实验室的合同延长了7年,直到2015年8月。第二次延长将MESA延长至2020年8月,并资助从2016年9月开始的第六次基本检查。该基本检查将通过附属研究资助的临床程序进行增强。最后12个月将用于结束研究和数据分析与发布(Austin et al., 2022; Bild et al., 2002; Burke, Lima, Wong, & Narula, 2016; Olson, Bild, Kronmal, & Burke, 2016)。
MRI预处理
T1w、T2w和流体衰减反转恢复(FLAIR)MRI使用N4偏场校正工具(Avants, Tustison, & Song, 2009)进行不均匀校正,该工具是高级归一化工具(ANTs)软件套件的一部分(http://stnava.github.io/ANTs)(Tustison et al., 2010)。使用偏场校正后的T1w图像生成解剖分割和脑掩模(Doshi et al., 2016)。这些图像使用FSL的FLIRT配准工具(https://fsl.fmrib.ox.ac.uk)(Jenkinson, Bannister, Brady, & Smith, 2002; Jenkinson & Smith, 2001; Greve & Fischl, 2009)刚性配准到参与者的SWI图像。来自MUSE的脑掩模用于T1w、T2w、FLAIR和SWI的去颅骨处理。
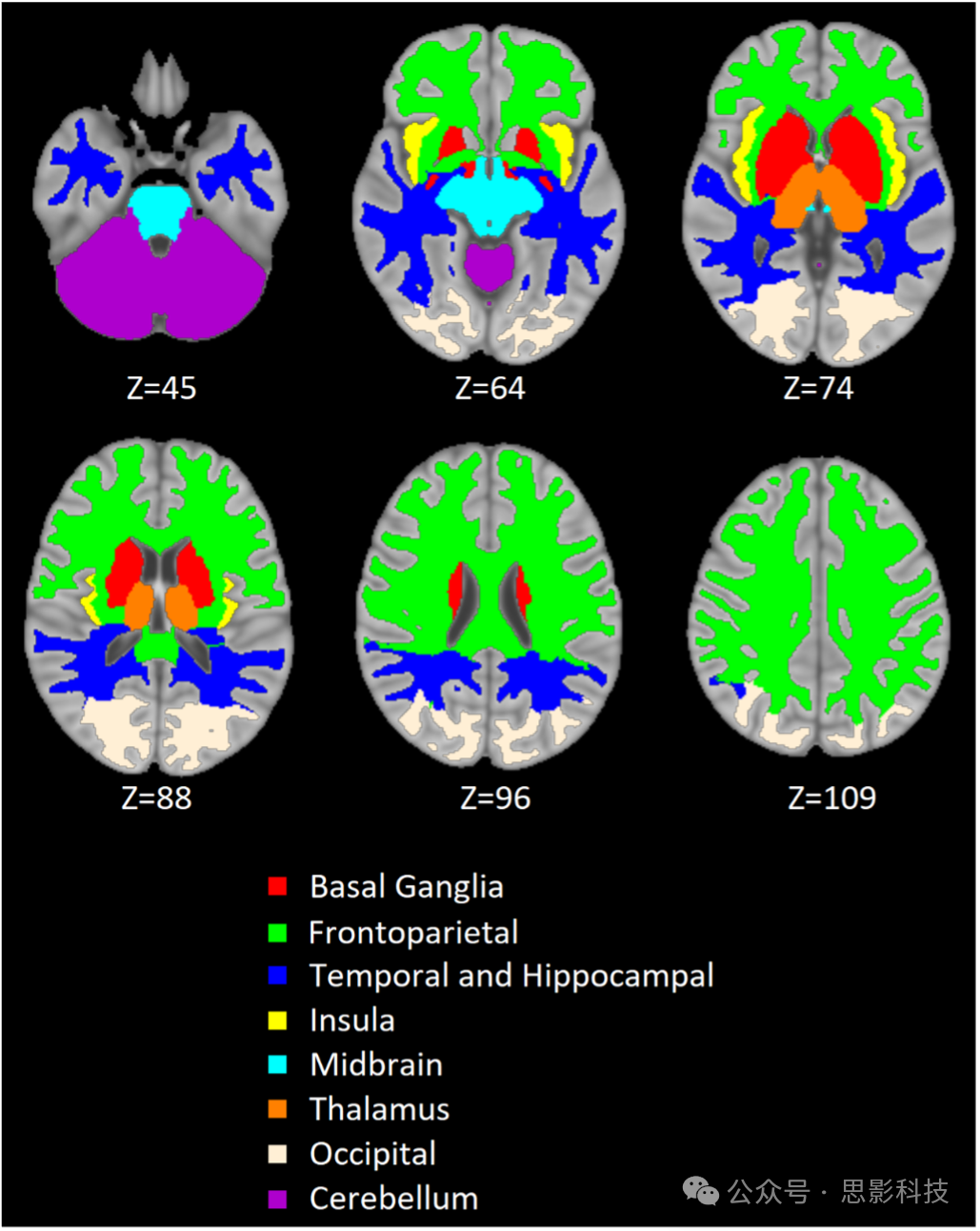
图S3基于现有MUSE分割的区域。
更多推荐
 已为社区贡献21条内容
已为社区贡献21条内容






所有评论(0)